Геморрагическая лихорадка с почечным синдромом (ГЛПС) —синонимы:
- Геморрагический нефрозонефрит;
- Эпидемическая геморрагическая лихорадка;
- Эпидемическая скандинавская нефропатия;
- Тульская, ярославская и др. геморрагическая лихорадка;
– острое вирусное природно-очаговое инфекционное заболевание, протекающее с высокой лихорадкой, выраженной общей интоксикацией, геморрагическим синдромом и своеобразным поражением почек в виде гломерулонефрита с нефротическим синдромом.
МКБ-10
Сокращение в тексте:
- БАВ – биологически активные вещества;
- ГЛПС – геморрагическая лихорадка с почечным синдромом;
- ДВС – диссеминированное внутрисосудистое свертывание;
- ИТШ – инфекционно-токсический шок;
- ОПН – острая почечная недостаточность;
- ОЦК – объем циркулирующей крови;
В России ГЛПС является наиболее часто встречающимся заболеванием из геморрагических лихорадок.
Первое описание заболевания, исторические сведения
Под различными названиями болезнь регистрировалась в районах Дальнего Востока с 1913 года. В 1935—1939 гг. военные врачи А. В. Чурилов и Г. М. Цыганков и др. наблюдали лихорадку, которая сопровождалась поражением почек и геморрагическим синдромом, были установлены основные клинические и патологоанатомические особенности болезни, предложены лабораторные тесты подтверждения диагноза, намечены пути лечения.
Впоследствии в 1941 г. А. В. Чурилов, профессор кафедры инфекционных болезней Военно-медицинской академии, впервые описал заболевание как самостоятельную нозологическую форму под названием «геморрагический нефрозонефрит».
Вирусная природа лихорадки была доказана еще в 1944 г. А. А. Смородинцевым, однако лишь к 1976 г. южнокорейскому ученому H. W. Lee удалось выделить вирус из легких грызуна. Вирус был назван Hantaan – по названию реки Хантаан. Похожие вирусы так же были выделены позже в Финляндии, США, России, КНР и других странах.
Этиология
Возбудитель ГЛПС – сферический РНК-содержащий вирус, диаметр которого составляет 85–110 нм. Вирус устойчив во внешней среде, способен длительно сохраняться при низких температурах.
Возбудитель геморрагической лихорадки с почечным синдромом относится к семейству буньявирусов – Bunyaviridae, которые включают около 30 серологически и отличающихся друг от друга генетически хантавирусов. Вирусы Bunyaviridae выделены в отдельный род.
В настоящее время описаны две клинические формы хантавирусной инфекции:
- ГЛПС:
- Вирус Hantaan – Хантанаан – возбудитель корейской геморрагической лихорадки;
- Вирус Puumala – Пуумала – возбудитель эпидемической нефропатии;
- Вирус Seoul – Сеул;
- Вирус Belgrad/Dobrava – Белград/Добрава;
- ХПС – хантавирусный пульмональный синдром: впервые описан в США в 1993 г. Возбудителем ХПС являются хантавирусы Sin Nombre, New-York, Black Greek Canal, Bayou, Laguna Negra, Andes.
Этиология
Возбудители геморрагических лихорадок относятся к вирусам пяти семейств:
- Аренавирусы:
- Являются возбудителями лихорадки Ласса;
- Вирусы Хунин (аргентинская лихорадка);
- Мачупо (боливийская лихорадка);
- Гуанарито (венесуэльская лихорадка);
- Сэбия (бразильская лихорадка);
- Буньявирусы: возбудители лихорадки долины Рифт и Крым — Конго;
- Флавивирусы, возбудители желтой лихорадки;
- Филовирусы, возбудители лихорадок Марбург и Эбола;
- Тогавирусы: возбудители лихорадки денге, кьясанурской лесной болезни и геморрагической лихорадки с почечным синдромом (ГЛПС).
Их геном представлен однонитевой РНК. Точность репликации генома вирусов данных групп проходит с низкой точностью, что обусловливает высокую частоту мутаций и появление новых вариантов вируса с измененной антигенной структурой и вирулентностью.
Из перечисленных инфекций в России встречаются следующие:
- Крым — Конго геморрагическая лихорадка (КГЛ);
- Омская геморрагическая лихорадка (ОГЛ);
- Геморрагическая лихорадка с почечным синдромом (ГЛПС).
Эпидемиология
Геморрагическая лихорадка с почечным синдромом (ГЛПС) относится к природно-очаговым зоонозам. По уровню и географическому ареалу заболеваемости в Российской Федерации занимает одно из ведущих мест среди инфекций с природной очаговостью.
Заболеваемость по регионам РФ
В 2006 году в 48 субъектах РФ было зарегистрировано 7200 случаев заболеваний, показатель заболеваемости – 5,0 на 100 000 жителей. Наибольшее число случаев регистрируется в Приволжском ФО – 6413 человек, что составляет 89 % от общего числа случаев заболеваний на территории РФ. По заболеваемости на 100 000 жителей наиболее высокие показатели отмечены на территории следующих субъектов РФ:
- Башкортостан – 71,2;
- Удмуртия – 37,0;
- Оренбургская область 22,9;
- Республика Марий-Эл – 21,1;
- Республика Татарстан 20,4;
- Ульяновская область – 17,2;
- Мордовия – 15,0;
- Самарская область – 11,4;
- Пензенская область – 9,9;
- Пермский край – 7,9;
- Нижегородская область – 6,6.
Уровень заболеваемости может варьировать от года к году, в основном это спорадические случаи, но периодически регистрируются эпидемические вспышки, иногда значительные.
Группы риска заражения
Считается, что заражению подвержены в большей степени мужчины, которые составляют до 3/4 заболевших. Это объясняется тем, что контакт с инфекцией особенно часто случается во время сельскохозяйственных и лесоустроительных работ, охоты, рыбалки, туристских походов, где среди присутствующего активного контингента мужчины составляют большинство. Чаще заболевают лица активного трудоспособного возраста 20—40 лет.
В зависимости от места заражения человека выделяют два типа очагов инфекции:
- Лесистый или внепоселковый. Заражение связано с кратковременным пребыванием в лесистой местности.
- Поселковый: заражение связано с поселением вблизи лесных массивов.
Во всех случаях отмечена тесная связь между заболеваемостью человека и численностью мышевидных грызунов в данной местности.
Более 65 % случаев заболеваний приходится на городское население. Заражение которого большей частью происходит на садовых и дачных участках. Заболеваемость лихорадкой сельского населения выше, но при этом в наиболее активных природных очагах геморрагической лихорадки с почечным синдромом, которые включают регионы Среднего Поволжья и Урала – показатель заболеваемости в крупных городах приблизительно в два раза выше, чем у сельских жителей тех же регионов.
В сельской местности наиболее высокий процент среди больных ГЛПС составляют работники сельского хозяйства: трактористы, механизаторы, шоферы, полеводы, животноводы, а в городах — промышленные рабочие и служащие.
Горожане заражаются в основном при работе на садовых и дачных участках, особенно на недавно отведенных для эти целей территории, где сохранен природный ареал переносчиков инфекции, на отдыхе в загородных оздоровительных учреждениях, посещении энзоотичных лесных территорий с целью туризма, охоты, рыбалки, сбора грибов и ягод, лекарственных растений. Туристические мероприятия часто сопровождаются ночевками в лесу, в пустующих постройках, заселенных грызунами, просто под открытым и т. п, где контакт с переносчиком заболевания наиболее вероятен.
Заражение на производстве происходит если промышленные предприятия или строительные площадки расположены в лесных массивах или неподалеку от них.
На территории России регистрируется только одна клиническая форма хантавирусной инфекции: ГЛПС.
Наиболее активные природные очаги геморрагической лихорадки с почечным синдромом регистрируются на Дальнем Востоке России (Приморский, Хабаровский края, Амурская область}, в Западной Сибири (Омская, Тюменская, Новосибирская области), на Урале.
Типы хантавирусов, циркулирующих на территории РФ
В России зарегистрирована и установлена циркуляция четырех патогенных хантавирусных типов. На европейской части возбудителем заболевания является в подавляющем большинстве случаев тип Пуумала, в азиатских регионах – тип Хантаан и Сеул. В последние годы отмечены случаи появления вируса Сеул в европейской части России. Особенностью этого вируса, имеющей важное эпидемическое значение, является способность к циркуляции среди домовых крыс.
Случаи геморрагической лихорадки с почечным синдромом наблюдаются на территории России на протяжении всего года, но закономерно отмечаются два сезонных подъема: весенне-летний и осенне-зимний. Подъемы связаны с нарастанием численности грызунов и увеличением количества контактов с ними населения. Наибольшее количество больных в европейских очагах геморрагической лихорадки регистрируется летом и осенью, а в очагах Дальнего Востока — осенью и зимой. В целом, для геморрагической лихорадки с почечным синдромом характерна летне-осенняя сезонность.
Источник возбудителя лихорадки
Быть резервуаром и источником возбудителя геморрагической лихорадки с почечным синдромом способны порядка 60 видов млекопитающих. Однако фактически основными резервуарами и источниками вируса, представляющих опасность заражения, являются грызуны следующих видов:
- Рыжая полевка;
- Полевая мышь;
- Серая и черная крысы;
- Разные виды серых полевок.
Инфицированный человек эпидемиологической опасности не представляет. Переболевшие приобретают пожизненный иммунитет.
В природных очагах Дальнего Востока России, Южной Кореи, КНДР, Китая, Японии отмечена циркуляция вируса Хантаан (Hantaan). Его основным носителем является полевая мышь.
Другой вариант вируса — Пуумала (Puumala), относится к европейским или западным, фиксируется в Финляндии, Швеции, России, Франции, Бельгии. Резервуар европейского варианта вируса – мышь рыжая полевка. В европейских регионах России зараженность рыжих полевок патогенным вариантом вируса в природных очагах может составлять до 40—60 %.
Передача инфекции
Механизм передачи инфекции
- Воздушно-пылевой (воздушно-капельный, через водную аэрозоль);
- Алиментарный;
- Контактный.
Пути передачи возбудителя
- Аспирационный;
- Пищевой и водный;
- Перкутанный – через поврежденную кожу и слизистые оболочки в лабораторных условиях.
Больные ГЛПС в эпидемиологическом отношении не опасны для окружающих.
Основными видами грызунов, с которыми ассоциируются заражения людей в России, являются:
- Рыжая, красная и красно-серая полевки;
- Полевая и восточноазиатская лесная мыши;
- Серая крыса.
Установленная инфицированность хантавирусом еще 42 видов мелких млекопитающих и 13 видов птиц, отловленных на территории России, эпидемиологическая роль которых в настоящее время изучается.
На активных очаговых территориях динамика заболеваемости ГЛПС характеризуется периодическими подъемами каждые 3—4 года, обусловленными периодичностью массовых размножений доминирующих видов грызунов и развитием среди них эпизоотий.
Патогенез
После внедрения в организм человека через поврежденную кожу и слизистые оболочки вирус локализуется в эндотелии сосудов и в эпителиальных клетках ряда органов, где происходит его репликация и внутриклеточное накопление. Затем наступает фаза вирусемии, что совпадает с началом болезни и появлением общетоксических симптомов.
Вирус оказывает выраженное капилляротоксическое действие, вызывая деструктивный артериит с повышенной проницаемостью сосудистой стенки, нарушением микроциркуляции, развитием ДВС-синдрома, все это сопровождается тяжелой полиорганной недостаточностью, особенно почек. Важная роль в развитии капилляротоксикоза принадлежит повреждающему действию иммунных комплексов. Помимо перечисленных эффектов вируса, развивается также поражение центров вегетативной нервной системы, ответственных за регуляцию микроциркуляции.
Поражение сосудов микроциркуляторного русла выражаются в деструкции стенок артериол, венул, капилляров, с нарушением микроциркуляции многих органов, в том числе почек.
Развитие и прогрессирование ДВС-синдрома обусловлено комплексностью воздействия повреждающих факторов:
- За счет капилляротоксического действия самого вируса на эндотелий микроциркуляторного русла;
- Определенная роль в развитии ДВС-синдрома принадлежит биологически активным веществам (БАВ): гистамину, серотонину, гиалуронидазы, компонентам калликреин-кининовой системы. Повышение уровня БАВ вызвано виремией и специфической интоксикацией.
- Накопление продуктов перекисного окисления липидов из эндотелиоцитов и тромбоцитов;
- Увеличение числа циркулирующих иммунных комплексов, активирующих систему комплемента, контактную фазу свертывания (через фактор Хагемана), т. е. присоединение иммунопатологического компонента;
- Нарушение реологических свойств крови, в том числе морфологические и функциональные изменения эритроцитов;
- Прямое повреждающее действие вируса на тромбоциты.
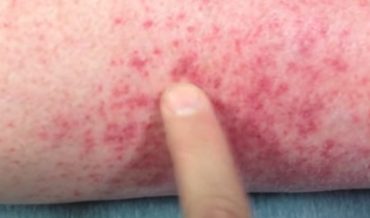
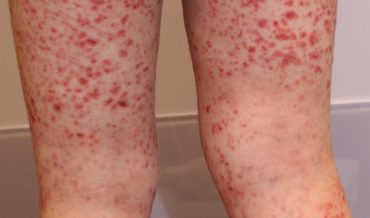
Весь этот комплекс приводит к развитию синдрома ДВС той или иной степени выраженности, лежащего в основе патологических процессов при ГЛПС. Как следствие повреждения сосудистой стенки развивается плазморея, уменьшается объем циркулирующей крови, повышается ее вязкость, что приводит к расстройству микроциркуляции и способствует возникновению микротромбов. Повышение капиллярной проницаемости в сочетании с ДВС-синдромом обусловливает развитие геморрагического синдрома, проявляющегося геморрагической сыпью и кровотечениями.
С одной стороны, синдром диссеминированного внутрисосудистого свертывания: (ДВС) является закономерным продолжением процессов нарушения микроциркуляции, центральной гемодинамики, с другой — синдром ДВС имеет собственные механизмы, посредством которых определяется исход заболевания. Синдром ДВС ответствен за клинические проявления геморрагического синдрома и острой почечной недостаточности при ГЛПС.
Результатом повышенной проницаемости через поврежденную сосудистую стенку являются плазморея в ткани, уменьшение объема циркулирующей крови, сердечного выброса и артериальной гипотензии, вплоть до развития ИТШ у части больных.
Острая почечная недостаточность
Острая почечная недостаточность (ОПН) при ГЛПС относится к ренальным (паренхиматозным) формам ОПН, вызванным поражением почечной паренхимы острым интерстициальным нефритом, развитие которого обусловлено разными механизмами:
- Нарушения микроциркуляции, повышение проницаемости сосудистой стенки, вызванные ДВС-синдромом, следствие – плазморея и серозно-геморрагический отек интерстиция почек с последующим сдавлением канальцев и собирательных трубочек. Интерстициальный отек усиливает нарушение микроциркуляции в почечной паренхиме вплоть до предельной ишемии с некрозом почечных канальцев. Нарушения микроциркуляции способствуют еще большему снижению клубочковой фильтрации и процессов канальцевой реабсорбции.
- Иммунопатологический фактор—фиксация иммунных комплексов на базальной мембране клубочков с их неминуемым повреждением, что также снижает клубочковую фильтрацию.
- Расстройства в центральной гемодинамике: снижение сердечного выброса, артериального давления, снижение ОЦК в свою очередь усугубляют нарушения почечного кровотока.
Лабораторные показатели при ГЛПС
Гиперазотемия
Мочевина. Повышение уровня мочевины происходит по нескольким причинам: избыточное поступление мочевины в кровь в результате ускоренного распада тканей (гиперкатаболические процессы), другая причина – недостаточное выведение азотсодержащих соединений с мочой за счет снижения экскреторной функции почек. Интенсивность катаболизма играет ведущую роль в начальном периоде заболевания.
Креатинин. Определение креатинина у больных ГЛПС указывает на глубину поражения паренхимы почек.
Нарушения водно-электролитного баланса
При ГЛПС чаще всего наблюдается гиповолемия, связанная с плазмореей и потерей жидкости со рвотой, но внеклеточной дегидратации сопутствует клеточная гипергидратация из-за снижения натрия крови и развития осмотической гипотонии крови.
Таким образом, при ГЛПС чрезвычайно важно знать количественное распределение жидкости между вне- и внутриклеточными секторами.
Дисэлектролитемия
- Повышение концентрации таких клеточных ионов, как магний, сульфаты, фосфаты, связано не только с нарушением их выведения, но и повышенным катаболизмом.
- Изменения клеточного калия не подчиняются этим закономерностям, ожидаемая гиперкалиемия наблюдается не всегда, возможна как нормокалиемия, так и гипокалиемия, так как калий может теряться через ЖКТ при наличии рвоты и диареи у больного.
- Концентрация плазменных ионов — натрия, хлора, кальция —обычно снижена вследствие перемещения их во внутриклеточный сектор и рвоты.
Гиперкалиемия
Гиперкалиемия — состояние опасное для жизни больного. При ГЛПС она развивается главным образом за счет усиления процессов катаболизма, дегидратации, ацидоза, водно-клеточной перегрузки.
Симптомы гиперкалиемии: парестезии, фибриллярные сокращения мышц, повышенные мышечно-сухожильные рефлексы, рвота, диарея.
Нарушения работы сердца, проявления на ЭКГ:
- Повышение, заострение зубца Т, снижение интервала $Т, зубцов Ри В, расширение комплекса QR$.
- Нарушения ритма и проводимости (аритмии).
- Снижение сократительной способности миокарда.
Повышение показателей гиперкалиемии происходит на фоне выраженного снижения показателей ионов натрия и кальция, которые являются антагонистами калия.
Нарушения кислотно-щелочного равновесия
Вследствие снижения или полного прекращения диуреза в крови повышается содержание нелетучих кислот: сульфатов, фосфатов, органических кислот — молочной, ацетоуксусной, пировиноградной и др. Развивается метаболический ацидоз со снижением буферных оснований. Частичная компенсация почечного ацидоза достигается повышенным выделением углекислоты через дыхательные пути, гипервентиляция создает условия для вторичного респираторного алкалоза, т. е. чем значительнее ацидоз, тем более выражена одышка у больных.
Олигурический период
В период олигоурии у большинства больных развиваются однотипные гуморальные нарушения:
- Страдает азотистый обмен;
- Нарастает внеклеточная дегидратация и клеточная гипергидратация;
- Усугубляются нарушения электролитного обмена;
- Растет метаболический ацидоз.
Полиурический период
При правильно проводимой терапии ОПН при ГЛПС переходит в следующую стадию — полиурии.
В полиурический период раньше всего повышается клубочковая фильтрация. Полиурия обусловливается осмотическим диурезом. Азотистые шлаки, накопившиеся в организме за время олигоурии, с восстановлением функциональной способности почек проявляют свое осмодиуретическое действие, причем количество выделяемой мочи не зависит от состояния гидратации организма; чрезмерные потери жидкости с мочой при недостаточном ее восполнении могут привести к обезвоживанию, гиповолемии и повторному развитию олигоурии.
Потеря кислых ионов с мочой в период полиурии способствует нормализации КОС, но может явиться причиной развития метаболического алкалоза.
Патогенетические механизмы повреждения микроциркуляторного русла лежат в основе других проявлений ГЛПС, в частности со стороны сердечно-сосудистой системы, ЦНС, эндокринной системы, органов пищеварения, кожи и слизистых, органа зрения.
Литература
Инфекционные болезни: национальное руководство под ред. Н. Д. Ющука, Ю. Я. Венгерова. – 3-е изд., перераб. и доп. – Москва: ГЭОТАР-Медиа, 2021.
Вирусные болезни человека / Ю. В. Лобзин, Е. С. Белозеров, Т. В. Беляева, В. М. Волжанин. – Санкт-Петербург: СпецЛит, 2015.
Геморрагическая лихорадка с почечным синдромом. Учебное пособие для ординаторов и интернов / В. Х. Фазылов, И. Э. Кравченко, Ф. А. Бабушкина – Казань; КГМУ, 2008.
Инфекционные болезни: учебник для студентов медицинских вузов Е. П. Шувалова, Е. С. Белозеров, Т. В. Беляева, Е. И. Змушко. – 7-е изд., испр. И доп. – Санкт-Петербург: СпецЛит, 2015.